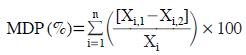Critical Evaluation of and Suggestions for the VOCs Measurement Method Established as the Korean Indoor Air Quality Standard Method
Copyright © 2014 Korean Society for Atmospheric Environment
During the last two decades, indoor air quality and volatile organic compounds (VOCs) have been of concern in Korean society due to their nature of potential health impacts. In order to investigate the pollution levels of VOCss in indoor environments, establishment of a solid test method for monitoring the airborne VOCss is essential. In Korea, a method based on adsorbent sampling and GC analysis coupled with thermal desorption was proclaimed as the Korea Standard Method for Indoor Air Quality Test. This study was carried out to examine some inherent problems of the VOCs measurement method. The VOCs method does not describe in detail preparing the standard samples. The standard samples may be prepared by impregnation of either liquid standard solutions or a mixture of standard gases. In this study, we investigated the optimal temperature condition for transferring the liquid standards onto a standard adsorbent tube. As a result, keeping the impregnation temperature at 250C will be recommended in regard of the boiling points of multiple target analytes and the thermal stability of the adsorbent. We also demonstrated some problems associated with handling of a syringe used for transferring the standard solutions onto the adsorbent tubes, and a best way to get rid of the syringe problems was suggested. Finally, a number of field works were conducted to evaluate the performance of adsorbent sampling methods. Comparison of different adsorbent tubes, i.e. tube packed with single sorbent (Tenax) and double sorbents (Tenax with Carbotrap), revealed that 30 to 40% differences between the two groups, implying that sampling efficiency is depending on the volatility and the strength of adsorbents. However, duplicate precisions for VOCs sampling with a same type of adsorbent and at same flow rates appeared to be satisfactory to be all within 20%, which is a quality control guideline. Distributed volume precisions were also found to be within a guideline value, 25%, although the precision was in general inferior to the duplicate precision. The Korea indoor VOCs test method should be more refined and improved in many aspects, particularly procedure and instrumentation for preparing the standard samples and specification of quality control assessment.
Keywords:
IAQ, VOCss, BTEX, Thermal desorption, GC/MS, Standard method1. 서 론
실내공기질은 우리나라에서는 90년대 후반부터 본격적으로 하나의 새로운 환경문제로 인식되어 왔다. 정부는 1989년 ‘지하공간 환경기준 권고치 설정’을 시작으로 1996년 ‘지하생활공간 공기질관리법’, 2004년 ‘다중이용시설들의 실내공기질 관리법’의 제정 이후 이들 관련법의 효과적인 시행을 위하여 2009년에는 정부 5개 부처가 합동으로 ‘실내공기질 관리 기본계획’이 마련된 바 있다(Korea Governmnet Working Group, 2009). 또한 관리대상오염물질의 확대를 위해 건축자재에서 방출되는 휘발성유기화학물질(volatile organic compounds, VOCs)로 인한 건강상 피해를 예방하기 위하여 다양한 실내환경에서의 VOCs 오염수준을 파악하기 위한 연구도 수행되었다(Kim et al., 2007; Baek and Kim, 1996). 실내에서 발생되는 오염물질은 비록 저 농도라 하더라도 거주자가 실내에서 보내는 시간이 길기 때문에 건강측면에서도 중요한 의미를 지니게 된다. 세계보건기구는 실내공기 중 VOCs에 대한 인체의 노출은 급성 및 만성 건강영향을 일으킬 수 있다고 발표한 바 있다(WHO, 2000).
실내공기질의 유지 및 관리를 위해서는 우선적으로 정확한 시료채취와 정밀한 분석을 통한 실내공기 오염물질의 종류와 발생원 및 해당오염물질의 발생량을 파악하는 과정이 필수적으로 요구된다(Shah and Singh, 1988). 다른 기준성 오염물질과는 달리 VOCs 그룹에는 이성질체를 포함하여 많은 종류의 물질이 포함되고 대체로 매우 낮은 농도로 환경 중에 존재하므로 정확한 측정자료를 얻기가 쉽지 않은 것으로 알려져 있다(Baek, 1996). 우리나라에서는 환경부 고시(제 2008-73호, 2009-223호를 거쳐 제 2010-24호로 개정고시)에 의하여 실내공기질 공정시험법이 법률로서 규정되어 있다 (Korea Ministry of Environment, 2010). VOCs 측정법은 시료채취방법에 따라 크게 흡착법과 용기법(캐니스터 및 테들러백)으로 구분되며 이들 두 방법은 상호보완적인 장∙단점이 있다. 이에 관한 보다 상세한 내용은 기존 문헌에서 찾을 수 있다 (Baek, 1996). 우리나라의 실내공기질 시험법에서는 주 시험법으로 고체흡착법을 채택하고 있다. 그러나 현행 VOCs 관련 시험법은 그 자체로 완벽히 정비된 상태로 보기는 힘든 몇 가지 문제점들이 있다(Seo et al., 2009; Kim, 2004). 특히 실험에 사용되는 표준시료의 제작과 정밀도 및 정확도의 평가방법에 있어서 모호한 부분이 많으며, 다양한 흡착제의 시료채취 성능을 충분히 설명하고 있지는 않은 실정이다.
본 연구는 실내공기 중 VOCs 측정을 위하여 고시된 우리나라 실내공기질 공정시험기준의 주 시험법인 고체흡착-열탈착-GC/MS분석법을 대상으로 시료채취와 분석 및 정도관리상의 문제점을 실제 실험실 환경에서 확인하고 이를 개선하기 위한 몇 가지 방안을 제시하기 위하여 수행되었다. 주된 연구내용으로는 VOCs 분석과 정량단계에서 가장 핵심적인 표준시료 제작 시 발생할 수 있는 오차유발요인과 시료채취용 흡착관의 성능 평가에 초점을 두었으며, 이들 두 요인은 결과적으로 정량된 VOCs 농도 자료의 정확성과 신뢰성을 부여하는데 핵심적인 정보이므로 시험법상의 문제점 규명 및 이를 개선하기 위한 과학적 정보 제공은 매우 의미가 있을 것으로 생각된다.
2. 재료 및 방법
2. 1 VOCs 시료채취용 흡착관
본 연구에서는 VOCs 측정을 위한 주 시험법인 고체흡착-열탈착법에 대한 문제점을 파악하고 개선방안을 강구하기 위하여 가급적 시험법에서 규정하고 있는 재료 및 방법과 최대한 유사하게 실험을 수행하였다. 공정시험법에서는 시료채취용 흡착제로서 약 200 mg의 Tenax-TA (60/80 mesh)를 충전한 흡착관을 사용하도록 지정하고 있다. 실내공정시험법에서는 n-헥산에서 n-헥사데칸까지의 영역에 포함되는 VOCs 물질의 정량이 목적이며 이 영역내의 물질들의 총합을 총휘발성유기화합물 (Total VOCs, 이하 TVOCs)로 정의하고 있다. 따라서 흡착제로서는 비교적 약한 극성(C6 계통)에서 비극성(C16 계통) 물질들을 채취하기 위하여 Tenax-TA를 채택하고 있다.
본 연구에서는 Tenax-TA (60/80 mesh) 300 mg을 충전한 1/4′′직경의 스테인리스스틸 흡착관 (단일 흡착관이라 칭함)과 함께 측정대상물질의 스펙트럼을 좀 더 확장하기 위하여 C4 탄화수소에서 C14 탄화수소까지 넓은 범위의 다양한 VOCs에 대해 우수한 흡착능과 탈착능을 가진 것으로 알려진 Carbotrap (20/40 mesh) 200 mg과 Tenax-TA (60/80 mesh) 100mg을 이중으로 충전한 흡착관 (이중 흡착관이라 칭함)을 병용하여 사용하였다. 이때 약한 흡착제인 Tenax를 전단에 배치하고 Carbotrap을 후단에 배치하였다(Oliver et al., 1995). Carbotrap은 Tenax-TA 보다는 약간 강한 흡착제로 알려져 있다. 따라서 C14 이상의 고분자 물질 (혹은 그에 상응하는 휘발성을 가진 물질)들의 선택적 포집 효율을 증대하기 위하여 Carbotrap 흡착제 전단에 Tenax 흡착제를 이중으로 충전하여 비교적 휘발성이 낮은 비극성 고분자 VOCs가 Carbotrap과 같은 강한 흡착제에 흡착되어 탈착 회수율이 저하되는 현상을 방지하고자 하였다 (Baek and Moon, 2004). 이들 흡착관의 구성과 흡착제의 특성은 각각 그림 1과 표 1에 나타내었다. 본 연구에서 사용한 이중흡착관은 이미 국내∙외에서 많이 사용되어 그 성능이 검증된 방법으로서 특히 독성 VOCs의 측정에 매우 보편적으로 이용되고 있다 (Baek et al., 2003; Ma et al., 1997; USEPA, 1997; Woolfenden, 1997; Baek and Kim, 1996).
2. 2 흡착관의 전처리
흡착관을 이용하여 시료채취를 수행하기 전에 clean-up 및 전처리 과정을 실시하였다. 본 연구에서는 흡착관 자동 전처리 장치인 TC-20 (Thermal Conditioner, Markers Inc., UK)을 이용하여 고순도 헬륨가스가 분당 80 mL/min으로 흐르는 조건 하에서 300°C에서 2시간 동안 전처리 과정을 수행하였다. 모든 흡착관은 전처리 후 1/4′′ swagelok 타입의 마개와 PTFE 패럴로 막고, 다시 이중 밀봉을 위해 septum이 달린 마개가 있는 50 mL 유리 바이알에 넣어서 실온에서 보관하였다.
2. 3 VOCs 표준물질
본 연구에서 표준시료 제작에 사용된 액상표준물질은 일본실내공정시험법 (Japan Ministry of Environment, 1997)에서 권장하고 있는 ‘52 component indoor air standards (Supelco, USA)’로서 자세한 내용은 표 2에 수록하였다. 액상표준물질 이외에 기기의 감도변화에 따른 보정에 필요한 내부표준물질(internal standards)은 d6-benzene, d8-toluene, d10-ethylbenzene, d5-bromobenzene 4종의 물질이 포함된 deuterated 물질(aldrich chemical, USA)을 사용하였다. 한편, 본 연구에서는 흡착관의 현장시료 채취성능을 평가하기 위하여 액상표준물질과는 별도로 VOCs 62종의 물질이 들어있는 기체상 표준혼합가스(공칭 1 ppm, Supelco, USA)를 사용하였는데, 이 표준물질은 미국 EPA TO-14 및 TO-15시험법의 전용으로 시판되고 있는 혼합 표준가스이다.
2. 4 VOCs 시료의 분석
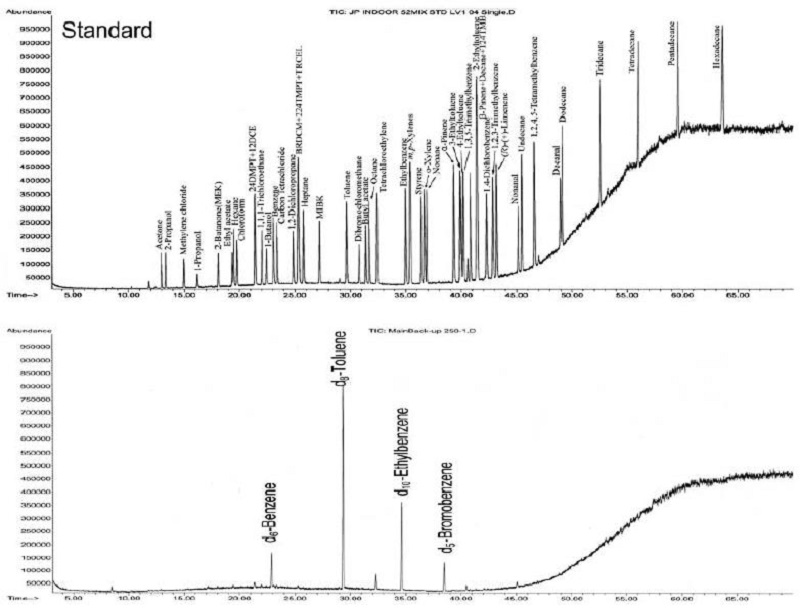
본 연구에서 VOCs 시료 분석에 사용된 열탈착장치와 GC/MSD의 사양과 운전조건은 표 3에 나타내었다. 열탈착장치의 운전 단계를 요약하면, 흡착관에 채취된 분석대상 VOCs가 1차적으로 300°C에서 약 50 mL/min의 유량으로 10분간 열탈착된다 (1차 탈착). 이때 운반 가스는 헬륨가스를 사용을 한다. 이렇게 탈착된 시료는 다시 -10°C의 저온응축트랩에서 5분간 농축된 후 약 5초 이내에 320°C까지 급속 가열되는 2차 열탈착을 통하여 GC의 모세관칼럼으로 주입된다. 열탈착 장치에서 2차 열탈착 이후 GC로 연결되는 transfer line의 온도는 180°C로 유지하여 2차 열탈착 이후 GC로 이동하는 동안에 시료의 손실이 생기지 않도록 하였다. 본 연구에서 사용한 열탈착 장치는 한꺼번에 100개의 시료까지 장착가능하며 연속적으로 시료를 분석할 수 있도록 되어 있다. 이와 같은 조건에서 표준용액과 내부표준물질을 분석한 일례는 그림 2에 나타내었으며 52가지 대상 물질 중 m-자일렌과 p-자일렌을 제외한 모든 물질이 분리됨을 알 수 있다.
2. 5 VOCs 분석의 정도관리
본 연구에서는 정도관리의 일환으로 개별 VOCs를 측정함에 있어 시료채취 및 분석에 사용된 흡착관/열탈착/GC/MSD의 전반적인 성능을 평가하기 위하여 재현성 및 검출저한계를 평가하였다. GC/MS를 이용한 분석방법의 재현성은 표준혼합기체시료를 대상으로 감응계수(response factor)에 대한 상대표준편차(relative standard deviation, 이하 RSD)로 평가하였다. 표준혼합기체시료를 이용한 외부보정법에 대한 재현성 평가는 표준물질 100 ng (benzene기준)을 흡착관에 함침하여 수행하였다. 일중 (within-a-day) 분석재현성 (n=10)과 일간(between days) 분석재현성(n=7)을 별도로 수행하였으며 그 결과는 표 4에 나타내었다.
일반적으로 특정 물질에 대한 검출저한계는 기기검출한계 (instrumental detection limits, 이하 IDL)와 방법검출한계 (method detection limits, 이하 MDL)로 구분하여 추정한다. IDL은 통상적으로 GC 크로마토그램상의 signal 대 noise의 비(S/N 비)를 기준으로 추정되어지며, 기본적으로 IDL은 GC분석에서 크로마토그램상에 나타나는 피크의 인정기준으로 적용되게 되므로 그 중요성은 매우 크다고 할 수 있다. 그러나 IDL에 의한 검출한계 추정은 분석당사자의 주관적 판단과 GC 운전조건 및 검지기의 감도에 따라 변할 수 있으므로 그 자체로 절대적이라고 할 수 없으며, 상대적인 의미가 크다고 할 수 있다. 반면에 USEPA에 의한 MDL 추정은 99%의 신뢰도(1%의 유의수준)로 분석대상물질의 최저농도가 영(zero)과 다르다고 보고할 수 있는 수준으로 정의된다(USEPA, 1990). MDL의 추정 방법은 보통 IDL의 3~5배 정도 되는 낮은 농도의 표준물질을 대상으로 최소한 7회 이상의 반복분석을 수행한 후 각 물질의 측정 농도에 대한 표준편차 (S.D.)를 이용하여 다음과 같은 식을 이용하여 계산한다(US EPA, 1990).
방법검출한계(MDL)=t (n-1, 0.01)×S.D.
여기서 t (n-1, 0.01)는 자유도 n-1, 1% 유의수준에서의 student-t 값이며 n은 반복분석횟수를 의미한다. 이와 같이 추정한 MDL이 주는 의미는 실제 분석기기상에서의 상대적인 검출한계가 아닌 분석 과정 전반에 내재된 불확실성을 고려한 검출한계에 대한 정보를 준다는 측면에서 VOCs 측정과 같이 여러 단계의 시료처리과정을 거치는 화학분석방법의 정밀성 (sensitivity) 평가에 적합한 것으로 알려져 있다 (Woolfenden, 1997).
본 연구에서는 저 농도 수준의 자료에 대한 신뢰성을 검증하기 위해 각 분석대상물질의 MDL을 추정하였다. MDL의 추정을 위해 분석대상물질 각 10 ng을 7개의 흡착관에 함침한 후 GC/MS로 분석하여 얻은 결과를 위의 식을 이용하여 계산하였으며, 그 결과는 표 4에 재현성 자료와 함께 나타내었다. 이와 같이 추정된 MDL 값을 기준으로 실제시료에 대한 공기채취량을 3 L로 가정하고 VOCs 농도로 환산하였다. 검출한계를 추정한 결과 대부분의 VOCs에 대하여 0.1~0.5 ppb의 범위로 나타났다. 부피농도로의 환산 시 물질별 분자량이 미치는 영향으로 인해 방향족 탄화수소 보다 유기염소계 물질의 검출한계가 상대적으로 높게 나타나고 있다. 검출한계이하의 자료처리에 대하여 아직까지 정립된 원칙은 없으나, 일반적으로 평균치 계산 등의 통계처리에서 검출한계 이하의 자료는 추정된 검출한계치의 절반 값을 대입하여 계산하기도 한다 (Hornung and Reed, 1990). 한편, 분석기기의 선형성을 확인하기위하여 1, 2, 5, 10 ppb (시료채취량 3 L 기준)의 표준시료를 각각 3회 분석 후 검량선을 검토한 결과 모든 측정대상물질의 상관성이 0.99 이상으로 만족할 만한 수준이었다.
3. 결과 및 고찰
본 연구에서 실험한 내용은 크게 두 가지 부분으로 구분된다. 첫째는 표준시료제조방법에 관한 내용이며, 두 번째는 흡착관의 시료채취 성능에 관한 내용이다. 우리나라 실내공기질 공정시험기준(ES 02602.1)에서는 교정용 표준흡착관을 제조하는 방법으로 액상표준용액을 이용하는 방법과 표준가스를 이용하는 방법 등 두 가지 방법을 설명하고 있다. 현실적으로는 교정용 VOCs 표준가스가 고가이므로 대부분의 실험실에서는 액상표준용액을 이용하는 방법이 선호되는 경향이 있다. 따라서 본 연구에서는 표준용액을 이용한 표준흡착관 제조 방법에 대하여 중점적으로 검토하였으며, 특히 함침 시의 온도 및 syringe를 이용한 함침방법의 문제점에 대하여 실증실험을 수행하였다. 흡착관의 시료채취 효능에 관한 실험은 실제 현장시료를 대상으로 서로 다른 흡착관의 비교실험과 동일한 흡착관에 대하여 서로 다른 유량으로 채취된 시료의 비교실험 결과를 다루고 있다.
3. 1 표준시료 제조시의 문제점 분석
현행 공정시험법에서는 액상표준용액을 흡착관에 함침할 때 “가스크로마토그래프 주입구에 흡착관을 연결한 후, 액상표준용액을 시료채취와 동일한 질량으로 흡착하여 교정용 흡착관을 만들어 사용하며 운반기체의 유속을 50~100 mL/min 정도로 맞춘다(환경부 고시 2010-24호)”라고 기술되어 있으며 이때 특별히 온도 설정에 대한 자세한 설명은 언급되어 있지 않다. 액상표준물질을 흡착관법으로 분석하기 위해서는 우선 표준물질을 기화시키기 위해 흡착관에 열을 가해주어야 한다. 이때 적정한 온도를 정해 주지 않는다면 흡착관에 흡착된 표준물질이 탈착되어 빠져나가는 파과현상 (지나치게 고온일 경우)과 함침장치 내부에 표준물질이 잔류되어 다음의 시료에 전이되는 carry over 현상 (지나치게 낮은 온도일 경우)이 나타날 수 있어 주의가 요망된다.
본 연구에서는 함침 온도조건에 따른 파과와 carry over가 일어나는지를 파악하여 적절한 함침 온도 조건을 찾고자 하였다. 이 때 휘발성유기화합물들의 끓는점을 고려하여 50°C, 150°C, 250°C의 3가지의 경우로 나누어 실험을 실시하였다. 먼저 syringe (10 μL, SGE, Australia)를 깨끗이 세척하고 액상 표준물질을 1 μL (벤젠기준 약 100 ng)를 분취하였다. Syringe로 표준물질을 분취한 다음 가스크로마토그래프의 충전관용 injector의 유출구 (1/4′′ 직경)에 전처리를 거친 깨끗한 흡착관 2개를 직렬 이단으로 연결하고 He 운반가스 유량 100 mL/min인 상태에서 injector에 액상표준물질을 주입하였다(그림 3). 흡착관을 이단 연결한 것은 액상표준물질이 기화하면서 파과현상이 발생하는가를 판단하기 위함이다.
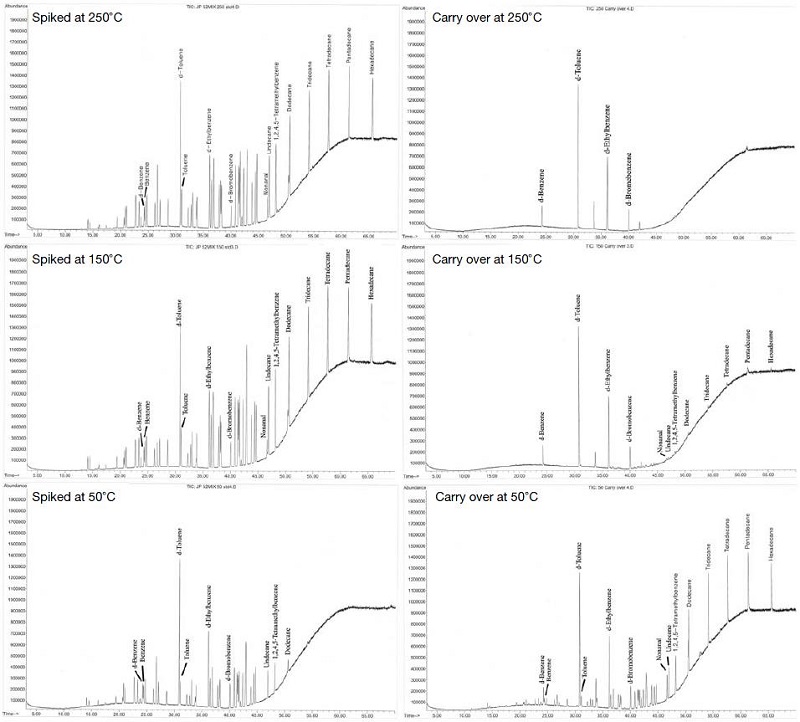
표준시료를 함침 받는 시간은 1분으로 하였으며 1분이 경과된 후 전단과 후단의 흡착관을 injector에서 분리하고 각각 Swagelok을 이용하여 양끝을 막고 다시 50 mL 유리 vial에 테플론 septum이 있는 마개로 닫아 분석 전까지 4°C로 유지되는 냉장고에 보관하였다. 표준시료가 주입된 흡착관을 제거하자마자 3번째 흡착관을 injector에 연결하여 250°C로 1분간 운반가스를 흐르게 하여 injector내의 잔류물질 유무를 확인하였다. 표준용액을 함침받은 모든 흡착관들은 내부표준물질(IS)을 주입하기 위하여 다시 injector에 연결하고 250°C에서 1분간 IS가 흡착되도록 하였다. 이러한 일련의 실험과정을 본 연구에서는250°C→150°C→50°C 순서로 각각 7차례 실시하였다. 이때 IS 주입으로 인한 액상표준물질의 시료 손실을 예상하여 IS 주입 시에도 깨끗한 흡착관을 표준흡착관 후단에 연결하여 별도로 분석한 결과 IS 주입으로 인한 파과현상은 없는 것으로 확인되었다. 실험과 실험 사이에는 injector 온도를 250°C로 올리고 메탄올 10 μL를 주입한 후 He가스를 충분히 흘려서 injector 내부를 세척하였다. 그림 4에는 서로 다른 함침온도에 따른 VOCs 표준시료와 injector 내의 잔존하는 물질의 carry over 현상을 확인한 실제 GC 크로마토그램의 일례를 나타내었다.
그림 4의 맨 위쪽 크로마토그램에서 볼 수 있듯이 액상표준물질을 함침 받은 표준흡착관과 표준흡착관을 제거한 후 바로 injector에 연결한 carry over 확인용 흡착관의 크로마토그램을 보면 250°C에서는 어떠한 carry over 현상도 발생하지 않은 것을 알 수 있다. 그러나 온도가 낮을수록 injector에서 기화되어 흡착관으로 이송되는 과정에서 고분자 물질일수록 충분히 기화되지 않고 injector 내에서 잔류되는 형상이 있음을 알 수 있다. 150°C에서는 7회 실험 중 두 번을 제외하고는 모두 carry over가 발생하였다. 전체 피크의 면적으로 환산할 경우 약 98% 정도가 표준흡착관으로 이송되며 C5이하의 저분자 물질은 약 1%, C10 이상의 고분자 VOCs는 약 10% 정도의 시료손실이 있었다. 따라서 150°C의 함침온도 역시 정확한 함침을 받기에는 문제가 있는 것으로 판단된다. Injector 온도를 50°C로 유지했을 때는 carry over 현상이 더욱 심하게 발생하였다. 면적비율로 볼 때 전체적으로 약 76% 정도의 액상시료가 표준흡착관으로 이송되며, 특히 후반부의 고분자 물질들은 거의 100% 기화되지 않는 것으로 나타났다. 반면에 250°C에서는 7회의 실험에서 모두 carry over 현상이 발생하지 않았다. 따라서 충전칼럼 injector를 이용하여 액상표준물질을 기화시켜 표준흡착관을 제조할 시에는 injector 온도를 최소한 200°C에서 250°C 범위로 설정하는 것이 적절할 것으로 판단된다.
본 실험에서는 액상표준물질을 주입하는 과정에서 사용하는 syringe에서 발생하는 문제점에 대하여 조사하였다. 일반적인 syringe는 전단부의 needle과 본체인 barrel, 그리고 용량을 조절하는 plunger의 세 부분으로 구성되어 있다. 실내공정시험법에 syringe needle의 dead volume에 대한 언급이 없으므로 일반적인 액상표준물질의 주입과정에서 dead volume을 고려한 실험은 거의 없다. 따라서 본 연구에서는 syringe needle의 dead volume을 고려한 경우와 그렇지 않은 경우로 나누어 실험하였다. 또한, syringe로 GC injector를 이용하여 액상물질을 주입할 때 실험자의 syringe 사용법에 의해 발생할 수 있는 문제점에 대해 추가 실험하였다.
본 실험에서 사용한 syringe의 dead volume은 0.6 μL로 나타났으며, 그림 5에는 이 syringe를 이용하여 각 물질의 농도가 100 ng/μL인 액상표준물질을 각각 1 μL (100 ng), 2 μL (200 ng) 및 5 μL (500 ng)을 주입한 표준흡착관을 분석하여 검량선을 작성하는 경우를 예시하였다. 그림 5의 왼쪽 그림은 dead volume (0.6 μL)을 제외하고 plunger로 빨아올린 용액 plug가 실제 barrel 상의 1 μL 눈금 (기준점)으로 부터 정확히 2, 3, 6 μL 눈금까지 걸쳐지도록 하여 100 ng, 200 ng, 500 ng을 주입한 경우이며, 오른쪽은 dead volume을 고려하지 않고 단순히 plunger가 barrel상의 눈금 1, 2, 5 μL에 도달한 상태에서 이를 각각 100 ng, 200 ng, 500 ng이라고 간주하고 작성한 경우이다. 그러나 후자의 경우에는 syringe의 dead volume에 사실상 0.6 μL(즉, 60 ng)이 포함되어 있으므로 결과적으로 주입되는 양은 160, 260, 560 ng이 될 것이다. 일례로 만약 분석대상물질의 peak 면적이 IS에 대한 면적비가 300인 경우의 어떤 물질의 질량을 위에서 마련된 검량선을 토대로 계산해보면, syringe의 dead volume을 고려하지 않는 경우 실제값의 약 74% (=184.3/247.6) 수준으로 낮게 산출될 수 있다. 이러한 오차는 저농도일 경우 더 크게 나타날 수 있으므로 각별한 주의가 요망된다. 따라서 현행 실내공기시험기준에서는 액상표준용액으로 표준시료를 제조할 경우 용액주입용 syringe의 dead volume으로 인한 오차유발 요인에 대하여 보다 면밀하게 명시할 필요가 있다.
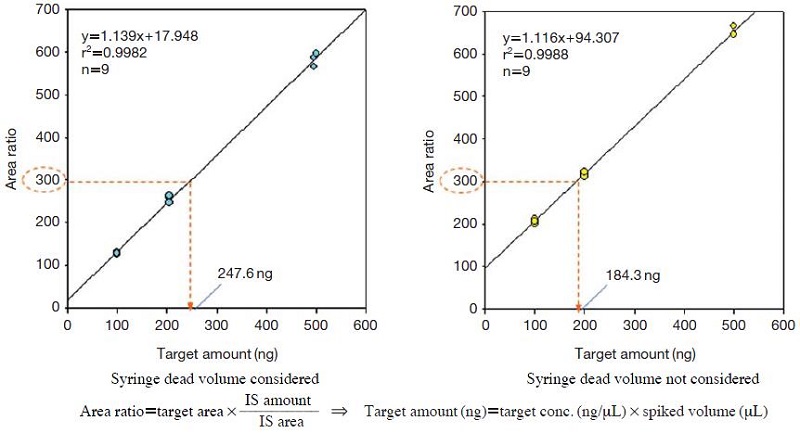
An example of calibration curves for the cases of syringe dead volume considered and not considered.
Syringe 사용 시의 또 다른 문제점은 실험자가 syringe를 사용하여 GC injector에 액상표준물질을 주입할 때 syringe의 취급방법에 따라 오차가 유발 될 수 있다는 점이다. 본 실험에서는 i) syringe의 plunger를 1회 pumping하고 바로 syringe를 뺄 때, ii) syringe의 plunger를 3회 pumping을 하고 뺄 때, 그리고 iii) syringe의 plunger를 3회 이상 pumping 하고 난 뒤 1분간 그대로 injector에 연결한 채로 두는 세 가지 경우로 구분하여 실험하였다. 각 실험을 18회 반복한 결과 실제 syringe에 남아있는 액상표준물질의 잔류량을 평균치 (±표준편차)로 표현하면 첫 번째 경우는 주입량의 약 35% (±8%)가 syringe에 잔류하였으며, 두 번째 경우는 약 13% (±4%)가 잔류하고, 세 번째 경우는 잔류량이 전혀 없는 것으로 나타났다. 따라서 액상시료 취급용 syringe는 표준용액의 기화가 종료될 때 까지 GC injector에 꽂아두는 것이 가장 적절하다고 할 수 있다.
실내공기질 공정시험법에는 기체상 표준물질을 이용한 표준흡착관 제조에 관하여 “정확한 정량을 위해서는 실제 시료와 비슷한 농도 수준인 저 농도의 휘발성유기화합물 표준기체를 흡착관에 각 성분의 흡착효율과 파과부피를 확인한 후, 교정용 흡착관을 만들어 사용한다. 가스를 이용하여 흡착관을 제조할 경우에도 액체를 소량 첨가하여 제조되는 흡착관과 동일하게 비활성 퍼지 가스를 100 mL/min로 흘려주고 적절한 표준 가스를 주입한다.”고 설명되어 있을 뿐 구체적인 장치와 방법에 대한 자세한 언급은 없다. 그러나 표준가스를 이용한다고 하더라도 실험자에 따라 기체상 표준물질의 흡착되는 양에 차이가 발생할 수 있다. 본 실험에서는 자체제작한 표준흡착관 제조장치 (그림 6)를 소개하고 그 방법을 설명하고자 한다.
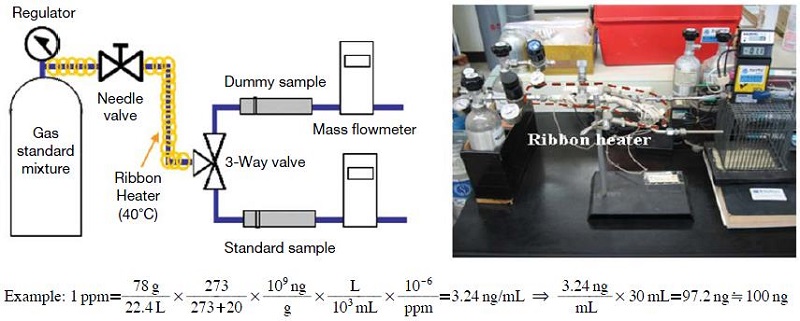
Schematic diagram of a self assembled apparatus for manufacturing the standard adsorbent tubes using a VOCs standard gas mixture.
일정한 농도의 기체상 표준물질을 이용하여 표준흡착관에 서로 다른 양이 흡착되게 하기 위해서는 함침시간을 고정하고 유량을 조절하는 방법과 유량을 일정하게 고정하고 함침시간을 조절하는 두 방법이 있다. 본 연구실에서는 시행착오를 통해 후자의 방법이 오차를 줄이는데 더 효과적이라는 것을 알게 되었다. 함침장치의 구성을 간략히 설명하면, 표준가스 실린더와 표준흡착관을 연결하는 관은 가급적 최단거리를 유지하도록 하고 리본히터를 이용하여 연결관을 최소 40°C 이상이 되도록 유지한다. 리본히터로 가열시키는 이유는 함침과정 동안 연결관 벽에 흡착이나 응결∙응축으로 인한 시료 손실이 생기지 않도록 하기위함이다. 표준가스 흐름은 3-way 밸브를 이용하여 먼저 표준흡착관과 동일한 dummy 흡착관으로 흐르게 한 후 needle 밸브를 조작하여 유량을 적정범위(대략 30 mL/min 범위)로 조정한다. 이때 유량계는 온도와 측정대상 기체(N2)가 보정된 질량유량계를 사용하는 것이 좋다. 흐름이 안정한 상태로 도달하면 3-way 밸브를 이용하여 기체의 흐름을 순식간에 전환시켜 표준흡착관으로 흐르게 하면서 이때부터 stop watch로 시간을 counting한다. 일례로 20°C인 실험실에서 1 ppm의 표준혼합가스 중 벤젠 약 100 ng을 채취하기 위해서는 표준가스의 흐름속도를 30 mL/min로 1분간 흐르게 하면 그림 6과 같이 양론적으로 흡착된 양을 계산할 수 있다. 고농도의 표준시료를 제조할 시에는 표준흡착관에서 파과현상이 일어나는지를 확인하기 위하여 동일한 흡착관을 이단으로 연결하여 후단의 흡착관에서 대상물질이 검출되는 지를 반드시 확인하여야 한다.
3. 2 시료채취용 흡착관의 성능 평가
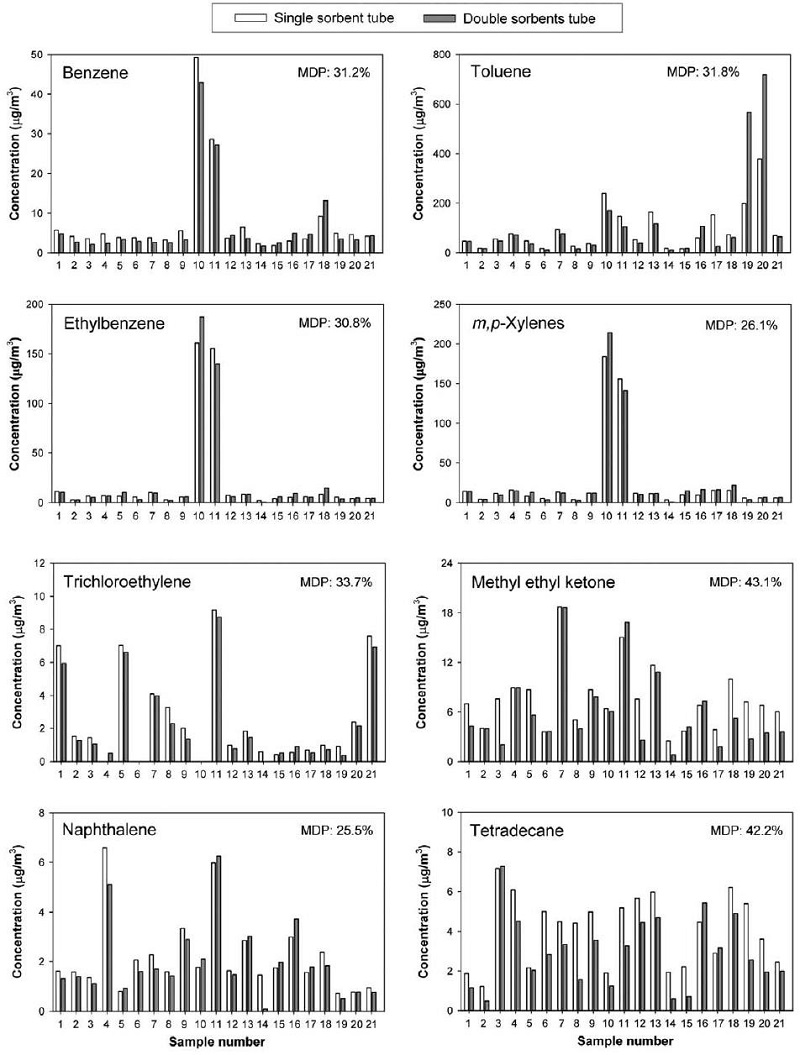
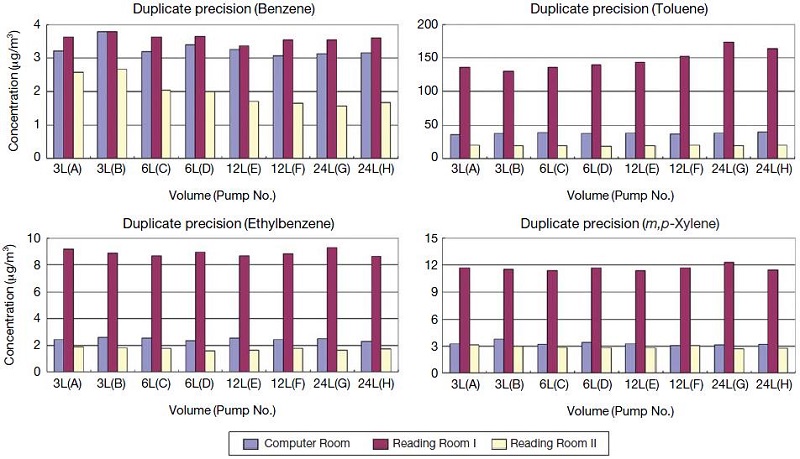
현행 실내공정시험법에서는 흡착관에 충전되어 있는 흡착제를 Tenax TA만으로 규정하고 있다. 흡착제 선정 시에는 채취효율, 흡착관의 회수율, 추출의 용이성, 열적 안정성 등을 모두 고려해야 한다. 여러 종류의 흡착제를 특성에 맞게 잘 조합하여 사용하면 의외로 분석대상물질의 종류도 다양하게 할 수 있으며 흡착관의 열탈착 성능도 증대할 수 있어 반복적으로 사용하는 흡착관의 수명과 성능 향상에 도움을 줄 수 있다 (Baek and Moon, 2004). 이러한 측면에서 본 연구에서는 Tenax TA 단일흡착관의 시료채취성능을 비교하기 위하여 실제 현장시료를 대상으로 이중흡착관 (Tenax-TA와 Carbotrap)과 비교실험을 실시하였다. 현장 시료는 법적으로 규정된 다중이용시설 17개 지점을 선정하여 100 mL/min의 유량으로 30분간 시료를 채취하였으며 총 21쌍의 중복시료를 채취하였다. 사용한 펌프는 Flec air pump 1001 (Chematec Inc., Denmark)로서 펌프에는 질량유량조절계가 내장되어 있어 일정유량을 유지할 수 있으며 펌프가 작동한 시간을 확인할 수 있는 기능도 있다. 다중이용시설에서 중복 채취한 시료를 분석하여 양자를 비교한 결과는 그림 7에 나타내었다.
많은 종류의 VOCs 중 검출빈도가 비교적 높고 농도도 높게 나타난 대표적인 VOCs 8가지에 대해서 비교한 결과 두 흡착관간의 시료채취 성능은 methyl ethyl ketone과 tetradecane의 일부 시료 쌍을 제외하고 전체적으로 유사하게 나타났다. 현행 실내공정시험법에서는 동일 장소에서 동일유량과 동일시간으로 시료를 채취한 평균중복정밀도(mean duplicate precision, 이하 MDP) 값이 20% 이내의 값을 가져야 한다고 명시하고 있다. 여기서 평균중복정밀도란 아래와 같이 계산된다.
여기서 Xi,1은 i번째 쌍의 시료 1의 농도, Xi,2는 i번째 쌍의 시료 2의 농도, Xi는 i번째 쌍의 시료 1, 2의 평균값이다. 그림 7에서 단일흡착관과 이중흡착관의 측정결과에서 차이가 발생하는 것은 임의오차 (random error)의 영향도 있겠지만 결국 흡착제의 특성에서 기인한 것으로 판단된다. 위의 결과를 놓고 볼 때 어느 쪽이 더 정확하다고 단정할 수는 없지만 일단 현장조사에서는 가급적 공정시험법에서 규정하고 있는 것과 동일한 종류의 흡착제를 사용하는 것이 보다 일관성 있는 자료를 제공해 줄 수 있다고 판단된다.
실내공정시험법에서 언급하고 있는 현장이중시료의 정밀도는 동일유량, 동일채취시간을 가정한 중복정밀도를 의미하고 있다. 그러나 중복정밀도는 동일시간대에 서로 다른 유량으로 채취한 시료의 편차도 평가되어야 한다. 공정시험법상의 권장 채취유량은 50에서 100 mL/min (약 2배 범위 이내)로 되어 있으나 실제 현장에서는 여러 가지 상황으로 서로 다른 지점에서 서로 다른 유량으로 시료를 채취하게 되는 경우가 많다. 이를 고려하여 미국 EPA TO-17의 정도관리 지침에서는 동일유량으로 동일시간에 시료를 채취한 경우에는 중복정밀도가 ±20%, 동일 시간에 서로 다른 유량 (약 4배의 범위 이내에서)으로 채취한 경우는 ±25%의 편차 이내가 되도록 명시하고 있다.
본 실험에서는 Tenax TA 단일흡착관을 사용하여 실내공정시험법에서 언급하고 있는 동일유량, 동일시간에 대한 중복정밀도를 평가함은 물론, 나아가 시험법에서 명시하고 있지 않은 서로 다른 유량에 대한 중복 정밀도도 조사하였다. 이를 위하여 25 mL/min 2대, 50 mL/min 2대, 100 mL/min 2대, 200 mL/min 2대로 총 8대의 펌프를 사용하여 각 2시간씩 실제 실내공기 시료를 채취하였다. 결과적으로 채취된 공기 유량은 각각 3 L, 6 L, 12 L, 24 L로서 이들 네 쌍의 측정결과를 상호 비교하면 동일유량과, 서로 다른 유량의 중복정밀도를 한꺼번에 평가할 수 있다. 실험은 사람의 이동이 없는 시간을 이용하여 대학교내 전산실(1회)과 도서실(2회)에서 이루어졌다. 이들 측정결과 중 일부(BTEX)를 그림 8에 예시하였다. 동일유량에 대한 중복정밀도는 모든 항목에서 20% 이내 수준을 만족하였으며 대부분이 10% 이내로 나타났다. 서로 다른 유량의 정밀도는 전반적으로 동일유량의 경우보다 떨어지는 것으로 나타났으나 벤젠의 일부 경우를 제외하고는 모두 25% 이내에 양호한 수준을 나타내었다. 벤젠의 경우 시료채취량이 3 L인 경우(2.7 μg/m3)와 12 L (1.7 μg/m3)인 경우 편차가 45.5%, 그리고 6 L (2.0 μg/m3)와 24 L (1.5 μg/m3)인 경우의 편차가 28.6%로 나타난 사례가 있었는데, 두 경우 모두 채취유량이 적을 때에 비해 유량이 많을 때 농도가 낮게 나타난 것으로 미루어 보아 BTEX 물질 중 가장 휘발성이 강한 벤젠의 경우 고유량에서 파과현상이 일부 발생했을 가능성이 있는 것으로 사료된다. 이렇게 파과가 발생했을 경우는 이를 방지하기 위하여 흡착관의 맨 뒤쪽에 Carbotrap이나 Tenax 보다는 강한 흡착제인 Carbopack-X 혹은 Carbosieve-SIII와 같은 흡착제를 back-up으로 충전하면 보다 광범위한 물질을 채취할 수 있을 것으로 예상된다. 그러나 공기 중에 수분이 많을 경우에는 강한 흡착제가 수분을 흡착하여 오히려 분석 재현성을 떨어뜨릴 수도 있으므로 상황에 따라 신중히 흡착제를 선택하여야 한다.
4. 결 론
본 연구에서는 국내 실내공기질공정시험기준 중 VOCs 측정방법의 몇 가지 문제점을 고찰하였으며 그 개선방안을 모색하였다. 실내공정시험방법에서는 VOCs 농도를 측정하기 위한 방법으로 고체흡착-열탈착-GC분석법을 주 시험법으로 하고 있다. 측정시험법에서 가장 중요한 단계는 표준시료를 이용한 정량단계이다. 그러나 현행 시험법에서는 표준시료 제조 시 표준용액과 표준가스를 이용하도록 언급은 하고 있으나 양자 모두 표준시료 제조시의 구체적인 방법에 대해서는 설명이 매우 미약하게 되어 있어 현실적으로는 실험자의 임의적 판단에 따라 오차가 발생할 수 있는 여지가 매우 많다. 본 연구에서는 특히 액상시료를 이용할 때의 함침 온도의 영향과 syringe 취급방법에 따라 예상치 못한 오차가 발생할 수 있는 가능성을 실증적으로 예시하였다. 결과적으로 함침온도는 최소 200°C 이상 250°C 수준이 가장 적합한 것으로 사료된다.
또한, syringe를 사용하여 액상표준용액을 주입할 경우 needle의 dead volume을 고려하지 않으면 1 μL 주입 시 약 60%의 오차가 발생할 수 있다. 따라서 본 연구에서는 액상표준물질을 이용할 때는 syringe의 dead volume을 제외한 양이 주입되도록 하는 방법을 제시하였다. 이외에도 실험자가 액상표준용액을 syringe로 주입하는 과정에서 충분히 기화될 때까지 plunger를 3회 이상 pumping하고 injector에 꽂은 채 1분간 대기한 후 syringe를 제거하는 것이 올바른 방법이라고 판단된다.
본 연구에서는 흡착관의 시료채취 성능을 평가하기 위하여 서로 다른 흡착관의 비교 및 동일한 흡착관에 대한 서로 다른 유량에서 채취된 시료의 분석을 통하여 실증적으로 중복정밀도를 평가하는 방법을 제시하였다. 실내공정시험법에서는 시료채취 과정의 정밀도에 대한 설명을 단순히 동일한 지점, 동일한 유량, 동일채취시간으로 시료를 채취하여 두 시료의 분석결과를 비교하는 것으로 언급되어 있으나 현실적으로는 동일한 조건에서 서로 다른 유량으로 채취된 두 시료의 정확성을 확인하는 내용이 포함되어야 할 것으로 생각된다. 국가가 지정하는 공정시험법은 반드시 최첨단 방법을 채택할 필요는 없다고 본다. 그러나 가장 보편적인 상황에서 누가 실험을 해도 정해진 재료와 수순을 따를 경우 허용 오차 범위 이내의 결과가 나올 수 있을 정도로 구체적이어야 한다. 따라서 현행 실내공기질공정시험기준 중 VOCs 측정시험법은 본 연구에서 검토된 몇 가지 사안들을 고려하여 보다 상세하고 표준화된 시험방법으로 개선되어야 한다고 사료된다.
References
- Baek, S.O., (1996), Sampling and analytical methods for the determination of volatile organic compounds in ambient air, J. Korea Air Pollut. Res. Assoc, 12(1), p1-13, (in Korean with English abstract).
- Baek, S.O., M.H. Kim, and Y.K. Seo, (2003), Evaluation of fugitive emission characteristics of airborne volatile organic compounds from different source categories, J. Kor. Soc. Atmos. Environ, 19(4), p363-376, (in Korean with English abstract).
- Baek, S.O., and Y.M. Kim, (1996), A study on the measurement of volatile organic compounds in indoor and ambient air of urban areas, J. Kor. Soc. of Environ. Eng, 18(2), p181-197, (in Korean with English abstract).
- Baek, S.O., and Y.H. Moon, (2004), Evaluation of adsorbent sampling methods for volatile organic compounds in indoor and outdoor air, Anal. Sci. & Tech, 17(6), p496-513, (in Korean with English abstract).
-
Hornung, R.W., and L.D. Reed, (1990), Estimation of average concentration in the presence of nondetectable values, Appl. Occup. and Environ. Hygiene, 5(1), p46-51.
[https://doi.org/10.1080/1047322X.1990.10389587]
- Japan Ministry of Environment, (1997), Guideline for Hazardous Air Pollutants Monitoring, p68.
- Kim, K.H., (2004), Consideration of the anlytical bias involved in the detection of total voaltile organic compounds(TVOCs), Anal. Sci. & Tech, 17(6), p489-495, (in Korean with English abstract).
- Kim, Y.S., Y.M. Roh, C.M. Lee, K.Y. Kim, J.C. Kim, and H.J. Jun, (2007), Pattern classification of voaltile organic compounds in various indoor environment, Kor. J. Environ. Health, 33(1), p49-56, (in Korean with English abstract).
- Korea Ministry of Environment, (2010), Ministry of Environment Announcement , No. 2010-24, March 5, 2014.
- Korean Government Working Group, (2009), Basic Plan for Indoor Air Quality, p171.
- Ma, C.Y., J.T. Skeen, A.B. Dindal, C.K. Bayne, and R.A. Jenkins, (1997), Performance ealuation of a thermal desorption/gas chromatographic/mass spectrometric method for the characterization of waste tank headspace samples, Environ. Sci. Technol, 31, p853-859.
- Oliver, K.D., W.A. McClenny, and E.H. Daughtrey, (1995), Analysis of VOCs in ambient air using multisorbent packings for VOCs accumulation and sample drying, J. Air Waste Manage. Assoc, 45, p792-800.
- Shah, J.J., and H.B. Singh, (1988), Distribution of volatile organic chemicals in outdoor and indoor air, Environ. Sci. & Tech, 22(12), p1381-1388.
- Seo, Y.K., J. Ye, M.K. Jeon, E.S. Son, and S.O. Baek, (2009), A critical evaluation of the standard method for indoor VOCs measurement, Proc. of 2009 Spring Conference, Kor. Soc. Atmos. Environ, p136-137.
- USEPA, (1990), Definition and procedure for the determination of the method detection limit, Code of Federal Regulations, Part 136, Appendix B, 537.
- USEPA, (1997), Compendium of methods TO-17, Determination of volatile organic compounds in ambient air using active sampling onto sorbent tubes, 2nd Ed, EPA/625/R-96/010b.
- WHO, (2000), Guidelines for Air Quality, Geneva, p180.
- Woolfenden, E., (1997), Monitoring VOCs in air using sorbent tubes followed by thermal desorption- capillary GC analysis, J. Air & Waste Manage. Assoc, 47, p20-36.